Số lượng nguyên tử của một nguyên tố liên kết với mỗi nguyên tử của nguyên tố khác trong phân tử được mô tả trong bảng hóa trị. Hóa trị là tính chất của một nguyên tố cho biết có bao nhiêu nguyên tử bổ sung có thể kết hợp với một trong các nguyên tử của nó trong liên kết cộng hóa trị.
Mục Lục
Bảng hóa trị là gì?
Bảng hóa trị liệt kê các electron hóa trị cho từng nguyên tố trong bảng tuần hoàn, xác định số lượng liên kết có thể có. Trong bài đăng này, chúng ta sẽ xem xét hóa trị là gì, cách tạo bảng hoặc biểu đồ hóa trị, cách tính hóa trị của một phân tử và cách sử dụng bảng hóa trị, cùng những thứ khác….
Dựa trên các electron hóa trị, đó là các electron ngoài cùng chịu trách nhiệm liên kết, nó mô tả cách một nguyên tố có thể hình thành liên kết. Có thể có từ một đến tám electron hóa trị, tùy thuộc vào loại nguyên tố. Điều quan trọng cần lưu ý là để bảng hóa trị được chính xác, các nguyên tố phải được sắp xếp theo thứ tự số nguyên tử….
Hóa trị có ý nghĩa gì?
Khả năng của một phần tử kết hợp với các phần tử khác được đo từ xa dưới dạng hóa trị của nó.
Thuật ngữ hiệu lực được đặt ra vào năm 1868 để mô tả cả tiềm năng rộng lớn của việc hợp nhất một nguyên tố và cường độ số của khả năng đó.
Nó được định nghĩa là số electron bị mất hoặc thu được bởi một nguyên tử trong một phản ứng hóa học hoặc số lượng electron được chia sẻ.
Hóa trị được đặc trưng là số lượng electron vì phần lớn liên kết được hình thành bằng cách trao đổi các electron hóa trị.
Trong hóa học, các electron hóa trị quyết định hóa trị là gì và chúng đại diện cho điều gì….
Ví dụ về hóa trị
Hóa trị của một nguyên tử là số lượng nguyên tử bổ sung mà nó có thể tạo ra một phân tử. Các chữ cái K, L, M, N, v.v. đại diện cho các quỹ đạo (vỏ) khác nhau trong đó các electron được sắp xếp thành nguyên tử. Các electron hóa trị là những electron nằm ở quỹ đạo hoặc lớp vỏ ngoài cùng của nguyên tử. Các electron hóa trị tham gia vào mọi quá trình hóa học vì quỹ đạo ngoài cùng của chúng thường chứa nhiều năng lượng hơn các electron ở các quỹ đạo khác.
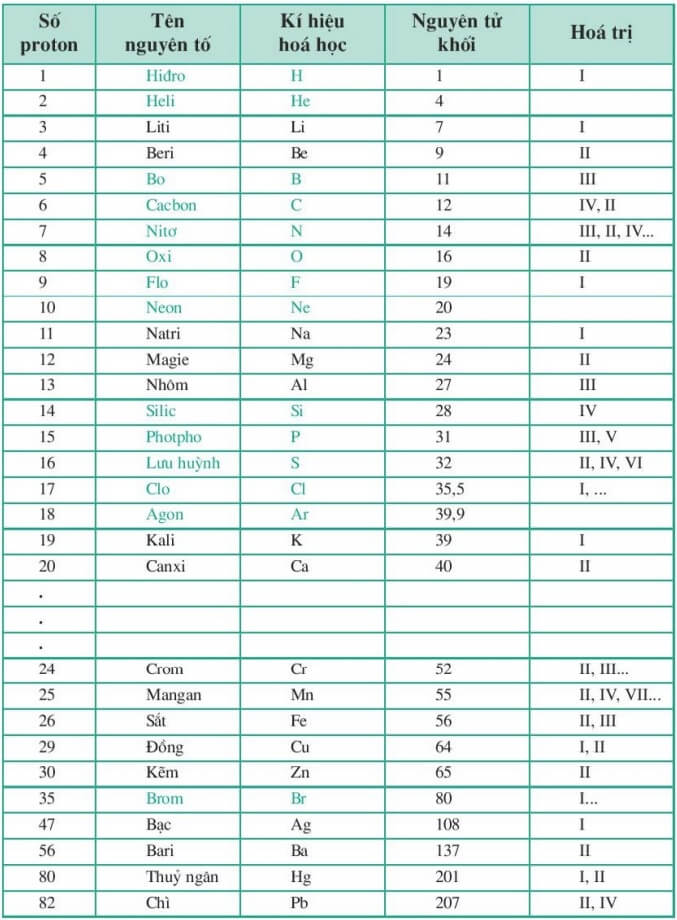
Hydro có hóa trị bằng một vì nó có thể tương tác với một nguyên tử khác để tạo thành phân tử.
Chúng ta có thể thấy chỉ có 6 electron hiện diện ở lớp vỏ cuối cùng của phân tử oxy. Bởi vì nó có thể tạo thành một phân tử với hai nguyên tử bổ sung, oxy có hóa trị bằng hai….
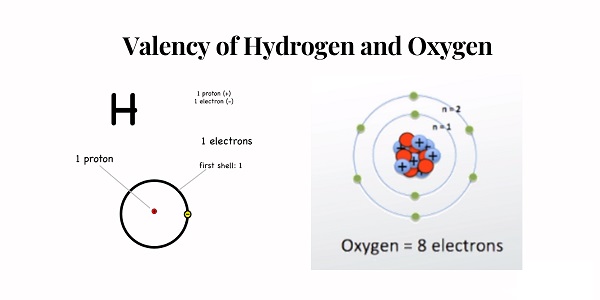
Lý thuyết của Bohr
Theo giả thuyết Bohr-bury, quỹ đạo ngoài cùng của nguyên tử có thể chứa tới 8 electron. Tuy nhiên, nếu quỹ đạo ngoài cùng được lấp đầy thì sẽ có rất ít hoặc không có hoạt động hóa học nào trong nguyên tố cụ thể. Khả năng hợp nhất của họ gần như không tồn tại…
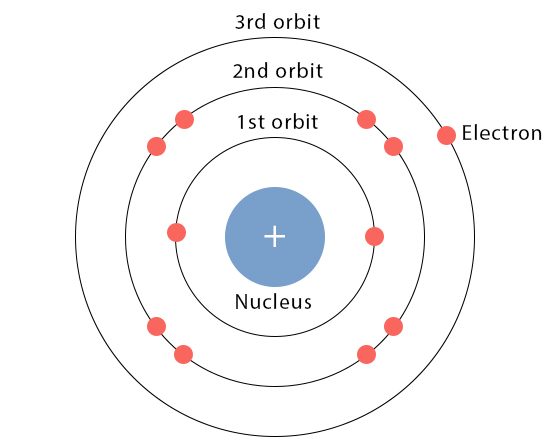
Cách tìm hóa trị của một nguyên tố?
Có ba phương pháp chính để xác định hóa trị của bất kỳ nguyên tố nào. Đầu tiên là quy tắc bát tử, công thức hóa học và bảng tuần hoàn.
Quy tắc bát tử
Chúng ta có thể đánh giá hóa trị của một phân tử bằng quy tắc bát tử. Nguyên lý này phát biểu rằng các nguyên tử của một nguyên tố hoặc hóa chất có xu hướng thu hoặc mất electron trong hợp chất mà chúng hiện diện, dẫn đến sự tăng hoặc giảm lượng electron ở quỹ đạo ngoài cùng của chúng. Số electron tối đa ở quỹ đạo ngoài cùng của nguyên tử là 8. Nếu một nguyên tử có 8 electron ở lớp vỏ ngoài cùng thì nó được coi là ổn định.
Công thức hóa học
Cách tiếp cận này, công thức biết giá trị từ công thức hóa học được xây dựng trên quy tắc bát tử. Có thể phát hiện ra hóa trị của nhiều nguyên tố hoặc gốc tự do chuyển tiếp trong một phân tử nhất định bằng cách quan sát cách chúng tương tác hóa học với các nguyên tố khác có hóa trị đã biết. Trong trường hợp này, quy tắc bát tử được sử dụng vì các phần tử kết hợp và gốc muốn đạt được tổng cộng 8 electron ở lớp vỏ ngoài cùng để chúng trở nên ổn định.
Bảng tuần hoàn
Bảng tuần hoàn các nguyên tố là công cụ phổ biến nhất được sử dụng để tính hóa trị trong phương pháp này. Tất cả các kim loại trong cột 1 đều có hóa trị +1, ví dụ như hydro, lithium, natri, v.v. Tương tự, tất cả các nguyên tố ở cột 17 đều có hóa trị 1, bao gồm flo, clo và các nguyên tố khác. Cột sắp xếp tất cả các khí hiếm. Các hóa chất này trơ và có hóa trị 0….
Bảng hóa trị hóa học lớp 7, lớp 8, lớp 9, lớp 10 đầy đủ
| Số nguyên tử | Tên nguyên tố | Hóa trị |
| 1 | Hóa trị của Hydrogen | 1 |
| 2 | Hóa trị của Helium | 0 |
| 3 | Hóa trị của Lithium | 1 |
| 4 | Hóa trị của Beryllium | 2 |
| 5 | Hóa trị của Boron | 3 |
| 6 | Hóa trị của Carbon | 4 |
| 7 | Hóa trị của Nitrogen | 3 |
| 8 | Hóa trị của Oxygen | 2 |
| 9 | Hóa trị của Fluorine | 1 |
| 10 | Hóa trị của Neon | 0 |
| 11 | Hóa trị của Natri | 1 |
| 12 | Hóa trị của Magie (Mg) | 2 |
| 13 | Hóa trị của Nhôm (Al) | 3 |
| 14 | Hóa trị của Silicon | 4 |
| 15 | Hóa trị của Photpho | 3 |
| 16 | Hóa trị của Lưu huỳnh | 2 |
| 17 | Hóa trị của Clo | 1 |
| 18 | Hóa trị của Argon | 0 |
| 19 | Hóa trị của Kali | 1 |
| 20 | Hóa trị của Calcium | 2 |
| 21 | Hóa trị của Scandium | 3 |
| 22 | Hóa trị của Titanium | 4 |
| 23 | Hóa trị của Vanadium | 5,4 |
| 24 | Hóa trị của Chromium | 2 |
| 25 | Hóa trị của Mangan | 7, 4, 2002 |
| 26 | Hóa trị của Sắt (Fe) | 2, 3 |
| 27 | Hóa trị của Cobalt | 3, 2 |
| 28 | Hóa trị của Nickel | 2 |
| 29 | Hóa trị của Copper (Cu) | 2, 1 |
| 30 | Hóa trị của Kẽm (Zn) | 2 |
